宅建業法 35条1項6号 「区分所有建物の国土交通省令等」の条文‐敷地,共用部分,専有部分,専用使用権,減免,維持修繕,管理費用,管理委託,維持修繕の実施状況
このページは、宅建業法 35条1項6号の全条文を挙げています。
なお、「区分所有建物うんぬん」ですが、正式なタイトルを記しておくと…、
『当該建物が建物の区分所有法に規定する区分所有権の目的であるものであるときは、契約内容の別に応じて国土交通省令等で定めるもの。』
…です。
全条文
①敷地に関する権利の種類及び内容
②共用部分に関する規約の定めがあるときは、その内容(その案を含む。)
③専有部分の用途その他の利用の制限に関する規約の定めがあるときは、その内容(その案を含む。)
④専用使用権(建物又は敷地の一部を特定の者にのみ使用を許すこと)に関する規約の定めがあるときは、その内容(その案を含む。)
⑤計画的な維持修繕費用、通常の管理費用その他の当該建物の所有者が負担しなければならない費用を、特定の者にのみ減免する旨の規約の定めがあるときは、その内容(その案を含む。)
⑥計画的な維持修繕のための費用の積立てを行う旨の規約の定めがあるときは、その内容及び既に積み立てられている額(その案を含む。)
⑦通常の管理費用の額
⑧管理が委託されているときは、委託先の氏名及び住所(法人:商号又は名称、主たる事務所の所在地)
⑨維持修繕の実施状況が記録されているときは、その内容
以下、「売買・交換」と「貸借」に、整理します。
「売買・交換」時の重要事項
「区分所有建物」の「売買・交換」時の重要事項ですが、先に挙げた①~⑨のすべてです。
冗長ですが、整理のため挙げると…、
①敷地に関する権利の種類及び内容
②共用部分に関する規約の定めがあるときは、その内容(その案を含む。)
③専有部分の用途その他の利用の制限に関する規約の定めがあるときは、その内容(その案を含む。)
④専用使用権(建物又は敷地の一部を特定の者にのみ使用を許すこと)に関する規約の定めがあるときは、その内容(その案を含む。)
⑤計画的な維持修繕費用、通常の管理費用その他の当該建物の所有者が負担しなければならない費用を、特定の者にのみ減免する旨の規約の定めがあるときは、その内容(その案を含む。)
⑥計画的な維持修繕のための費用の積立てを行う旨の規約の定めがあるときは、その内容及び既に積み立てられている額(その案を含む。)
⑦通常の管理費用の額
⑧管理が委託されているときは、委託先の氏名及び住所(法人:商号又は名称、主たる事務所の所在地)
⑨維持修繕の実施状況が記録されているときは、その内容
…となっています。
貸借時の重要事項
次に、「区分所有建物」の「貸借」時の重要事項は、「2つ」あって…、
③専有部分の用途その他の利用の制限に関する規約の定めが“あるとき”は、その内容(その案を含む。)
⑧管理が委託されているときは、委託先の氏名及び住所(法人:商号又は名称、主たる事務所の所在地)
…となっています。
| カテゴリー: 宅建 | Tags: 宅建, 宅建‐宅建業法, 宅建業法‐35条(重要事項の説明) | 2020年2月1日 1:16 PM |
| ▲ Back to Top. | ▲ Back to Homepage. |
令和1年度(2019年度)の宅建試験の「科目別」総評
このページは、「令和1年度(2019年度)の宅建本試験」の「全体的な傾向・特徴」を解説しています。
んでは、科目別に、R1年度の宅建試験を見ていきます。
権利関係
「権利関係」ですが、出題数の「14問」に、変わりはありませんでした。
「民法」で「10問」、「借地借家法」で「2問」、「区分所有法」で「1問」、「不動産登記法」で「1問」と、例年通りでした。
民法‐権利関係
「権利関係」の「民法」ですが、近年の問題と比べると、比較的、点の取りやすい問題が多かったです。
基本的な条文知識や判例知識があれば、多くの問題が取れたはずです。
もちろん、難しい問題・難しい選択肢が相変わらず登場します。
たとえば、「7問:債務弁済」です。
よくわからない選択肢があり、解答は厳しいです。しかし、基礎レベルの選択肢もあるので、ギリギリまで、選択肢を絞れたように思います。運よく、1点取れた人もいるはずです。
さて、当該年度の「民法」の目玉は、やはり、典型的な「過去問」の「使い回し」でしょう。
「10問:抵当権譲渡」なのですが、H27にも、同様の出題があり、「宅建は、過去問」との思いを、再認識した次第です。
ここまでストレートではないですが、過去に出た選択肢が、形を変えて出題されるこことはよくあります。
過去問に出た問題は、“とりあえず”でもいいので、解けるようになっておきましょう。
なお、「民法」ですが、R2以降、「改定」を控えています。
問題文・答え・解説ともに変わってくるので、過去問演習時は注意してください。
借地借家法‐権利関係
「2問」出題の「借地借家法」ですが、本年度も、オーソドックスな出題でした。
キチンと勉強した人なら、安定して、「2問」取れたはずです。
難科目の「税法」等に比べたら、圧倒的に取りやすいのが「借地借家法」です。
例年、出るところは、決まっています。
大概、民法との比較問題や、定期借地権・定期借家権が問われるので、集中的に勉強して、得意科目にしておきましょう。
区分所有法‐権利関係
「1問」出題の「区分所有法」ですが、選択肢のすべては基礎レベルで、まったく問題なかったはずです。
例年、「区分所有法」は、カンタンな問題なので、優先して勉強してください。
不動産登記法‐権利関係
「不動産登記法」ですが、今年も、相変わらず、難しいです。
分筆登記・合筆登記が問われましたが、この論点がテキストに載ってなかった受験生も、多くいたと思います。
また、見たこともないような条文(不動産登記法 第17条 代理権の不消滅)が出題されており、受験生をウンザリさせたはずです。
例年、「不動産登記法」は、難しいです。
過去問の「使い回し」も少ないので、「後回し」にして、宅建業法等の頻出論点に尽力しましょう。
法令上の制限
「11問」出題の「法令上の制限」ですが、ざっくり言うと、「この年度に当たった受験生はラッキー」です。
難問が少なく、近年と比べると、圧倒的に、点数が取りやすい年度でした。
まず、「都市計画法」が実にオーソドックスな出題(超絶ド定番の「地域地区」と「開発行為」)で、2問丸々取れた受験生も、たくさんいたと思います。
宅地造成等規制法、土地区画整理法、農地法、国土利用計画法、地価公示法も、ひねくれた問題や、枝葉末節の問題もなく、過去問演習を繰り返した人・テキストを精読した人なら、まったく問題なく点が取れたはずです。
当該年度の過去問演習に際しては、先の都市計画法、宅地造成等規制法、宅地造成等規制法、農地法、国土利用計画法、地価公示法は、ぜんぶ取れるくらいに勉強してください。
どれも、超絶基本レベルです。解けないのは、勉強不足の証です。
さて、「税法」は、相変わらず、費用対効果が低かったです。
「建築基準法」は、なんのこっちゃ?!の出題でした。
「税法」と「建築基準法」は、例年通り、「難」でした。
とはいえ、過去問の「使い回し」に備えて、チェックだけはしておきましょう。
宅建業法
「20問」出題に、変わりはありませんでした。相変わらず、宅建のメイン科目です。
R1の「宅建業法」ですが、強いて言えば、「やや難しい」です。
当該年度の「宅建業法」は、近年に比べると、手強い問題が目立ちます。
「国土交通省令で定める事項」の細かい規定を、しかも、「賃借」のを問う「28問:宅建業法:35条問題」。
「罰金」の正確な判断ができないと正解できない「29問:宅建業法:監督処分・罰則」。
「改正問題」の「32問:宅建業法:報酬」。
これらのハイレベルの問題は、そこそこ勉強した受験生でも、なかなか、正解には辿り着けなかったように思います。間違えても、やむなし、といった次第です。
しかしながら、他の問題では、定番問題・頻出問題も多く、キチンと勉強した受験生なら、これらを取ることで、致命的な失点には到らなかったかと思います。
まあ、有体に言えば、他の科目の問題が、比較的、点が取り易かったので、“点数調整”的なしわ寄せが「宅建業法」に及んだ、とも言えるでしょう。
今後とも、「宅建業法」は、少しずつ難化していくように思います。
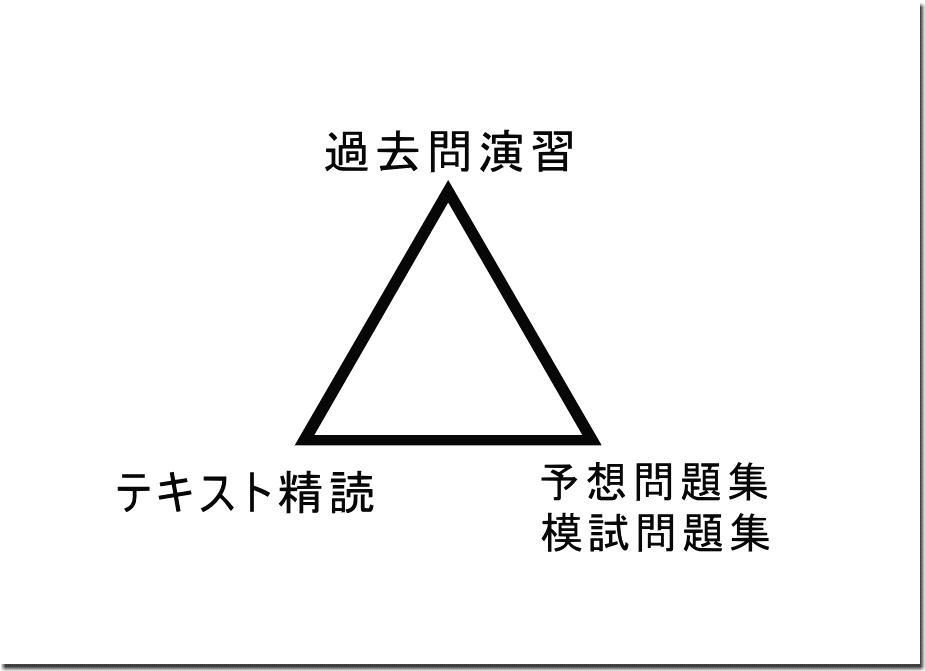
当該年度の「宅建業法」で苦戦した人は、上記画像のように、過去問演習と、テキストの精読に加え、予想問題集・模試問題集で、問題演習の「数」を稼いでおきましょう。
「宅建業法」は、やはり、問題演習の「数」が、一番、物を言います。
その他
「その他」ですが、例年通りでした。
「統計」は、相変わらずの数字暗記が必要です。時間がない人は、直前に、予想問題集や模試問題集の数字を押えましょう。
「土地・建物」は、過去問レベルで、ゼッタイに取らない難易度です。
「住宅金融支援機構」も「景品表示法」も、過去問レベルでした。
「統計」を除く「その他」の4問は、キチンと勉強したなら、まず取れる「得点源」です。
「その他」の全問正解は厳しいですが、「4問取って4点」を、目標にしてください。
| カテゴリー: 宅建 | Tags: 宅建 | 2020年1月18日 10:27 AM |
| ▲ Back to Top. | ▲ Back to Homepage. |
令和1年度(2019年度)の宅建試験の「全体」総評‐ソフトひっかけ あらわる等
このページは、「令和1年度(2019年度)の宅建本試験」の「全体的な傾向・特徴」を解説しています。
んでは、本編です。
数字から見るR1‐合格率とか
令和1年度(2019年度)の宅建試験ですが、申込者数「276,019人」で、受験者数「220,797人」で、合格者数は「37,481人」となりました。
合格率は「17.0%」、合格基準点(一般)は「35点」でした。
ちなみに、昨年の平成30年度(2018年度)は、申込者数「265,444人」、受験者数「213,993人」、合格者数は「33,360人」、合格率が「15.6%」で、合格基準点(一般受験者)が「37点」でした。
R1年度は、昨年と比べて、合格者数が4,000人も、増加しています。
R2の受験生にはアレですが、過去のデータを見ると、ある年度に合格者が増加したら、翌年は「減る」ことが多いです。
しかも、H28・H29・H30・R1と、近年ずっと合格者が増加しており、翌年以降に、引き締める「可能性」があります。
R2は、合格者数が35,000人を切るおそれもあります。
やることさえやれば合格できる宅建ですが、油断せず、「少し厳しいかも」と、気を引き締めて臨むべきかと思います。
R1試験の全体的な傾向
R1試験の全体的の傾向は、「ほぼ例年」といった寸法です。
試験問題は、全体的に、それほど難しくなかったです。
そのためか、前年に比べ、合格率が約2ポイントも高くなりました。「17%」に達したのは、H26から“5年ぶり”です。
新手の傾向
令和1年度(2019年度)の試験ですが、傾向(特徴)を挙げると、3つあって…、
①「ソフトひっかけ」
②「難易度の平準化」
③「やっぱり宅建は、過去問」
…となっています。
以下、ざっくり、上記3点を見ていきます。
①「ソフトひっかけ」あらわる
以前から、“似たような現象”はあったのですが、「ソフトひっかけ」とも言うべき、“ゆるい「ひっかけ」が如実に散見されます。
代表的なのは…、
「第36問:宅建業法:37条問題・・・選択肢ア」といった選択肢です。
一口で言えば、「突拍子のない内容」の選択肢なのですが、一読しても、(なんだこりゃ?!)的に、頭が真っ白になるものとなっています。
出題者が「ソフトひっかけ」を繰り出す意図としては、「受験生を混乱させる」ことだと思います。
ガチの「ひっかけ」ではないので、配偶者のような極悪さはありませんが、新手のタイプなので、動揺しないなどの注意が必要です。
今後の試験では、(何いってんの?これ、「ソフトひっかけ」じゃないの?!)的な判別が増えるかもしれません。
対策としては、テキストを精読し、知識を整理しながら、正確に憶える、です。
②「難易度の平準化」
当該年度の試験問題ですが、突出した難問は出ていませんが、選択肢の1~2つを難しくして、個々の難易度を、“平準化”した感じの試験問題となっています。
まず、選択肢のすべてが難しい「ガチ難問」が出なくなっています。
当該年度では、H30のような「一目で解けないとわかる難問」が影を潜めています。
参考:平成30年度(2018年度)宅建の過去問+解説インデックス
先に述べたように、当該年度は、1問中に難儀なガチ選択肢が1~2つ登場する、といった構成が目立ちます。
このため、難問であっても、判別可能の選択肢もあり、多少は、正解に“肉薄”できた受験生が多かったように思います。
キッチリ勉強した受験生なら、難問とはいえ、そこそこ点数にしたのではないかと、推測します。
個人的には、当該年度の試験は、いい仕事をしていると思います。(洗練されたなー)と思っています。
見るからに、即、「捨て問」となる難問を出すよりも、当該年度のように、受験生がせめて一太刀できる難問の方が、『試験』になると思います。
もちろん、今後の試験で「難易度の平準化」が続くかどうかは不明です。
ですが、難問といえども、「即、諦めないで、目を凝らして、解ける選択肢だけでも解く」ことは、重要な試験戦術かと思われます。
③「やっぱり宅建は、過去問」
手短に言いますが、やはり、「宅建の根幹は、過去問」です。
過去問演習では、(もう、こんなん、出ないだろー)という考えは、危険です。
具体的な例は、「第10問:抵当権譲渡」です。
当該「抵当権譲渡」の論点は、H27にも出題されており、油断せず過去問演習をした人なら、ラクラクと「1点」が取れたはずです。
参考: H27-7問 抵当権の譲渡、放棄
実は、わたし、H27の第7問を見たとき、(こんなクソ問題、金輪際、出ることはないな)と思ったのです。
(完全に捨ててよい)と確信していたのですが、蓋を開ければ、4年後に、再登場したのでした。
R1の第10問を見たときは、洗面所で配偶者とかち合ったときのように、仰天しました。
正直なところ、わたしが現役の受験生だったら、この第10問を落としたことで、不合格になっただろうと、実感しています。そのくらい、致命的な「失点」となったはずです。
宅建は、本当に、過去問を甘く見てはいけない、と再認識しました。
当該第10問に限らず、試験問題の全体を見ても、そこかしこに、「過去の出題実績」のある選択肢が登場しています。
過去問さえシッカリ繰り返していれば、「過去問の使い回し」の選択肢が判別できて、あとは、適当に選んでも、半々(50%)で正解できるという問題は、結構あります。
当該年度の傾向を踏まえ、皆さんも、「過去問に出たものは、ゼッタイに、甘く見てはいけない。安易な判断は、厳禁。必ず、チェックだけはする。解けるようになっておく。」と、肝に銘じてください。
やっぱり、宅建は、過去問です。
繰り返します。
最も点数を上げる勉強が「過去問演習」です。
アドバイス的なこと‐確実な合格を目指して
R1試験も、宅建試験の原則に則った出題でした。
つまり、「テキストを精読し、過去問演習を繰り返す」ことで、穏当に合格できる、といった塩梅です。
ただ、過去問演習だけでは、対応のできない、新手の問題・論点が、ゾクゾクと、登場しています。
特に、「宅建業法」で、それが顕著です。
そこで、ある程度、過去問演習が進んだら、模試問題集・予想問題集で、さらに問題演習の数を稼ぐことを、勧めます。
過去問演習とテキスト精読で、点数の取りこぼしが防げます。
んで、模試問題集・予想問題集で、さらなる問題演習をすることで、新手の出題にも、対応できるようになります。
先に挙げた「三角形」が、“合格する”宅建の試験勉強です。
「科目別総評」に、続きます。
| カテゴリー: 宅建 | Tags: 宅建 | 2020年1月18日 10:19 AM |
| ▲ Back to Top. | ▲ Back to Homepage. |