登録販売者 第5章:適正使用
第2節:医薬品の安全対策
第2項:医薬品による副作用等が疑われる場合の報告の仕方
2 医薬品による副作用等が疑われる場合の報告の仕方
「法の規定に基づく医薬品の副作用等報告(※1)では、保健衛生上の危害の発生又は拡大を防止するためとの趣旨に鑑みて、医薬品等(※2)によるものと疑われる、身体の変調・不調、日常生活に支障を来す程度の健康被害(死亡を含む。)について報告が求められている。」
「なお、医薬品との因果関係が必ずしも明確でない場合であっても報告の対象となり得る。」
「また、安全対策上必要があると認めるときは、医薬品の過量使用や誤用等によるものと思われる健康被害についても報告がなされる必要がある。」
注記‐(※1)
開ける
『医療機関等からの医薬品、医療機器又は再生医療等製品についての副作用、感染症及び不具合報告の実施要領の改訂について」の別添「「医薬品・医療機器等安全性情報報告制度」実施要領」により実施方法が示されている。』
まあ、これは試験に出ないね。無視していいでしょう。知らんがな、でおしまい。
注記‐(※2)
開ける
『医薬部外品又は化粧品による健康被害についても、自発的な情報協力が要請されている。なお、無承認無許可医薬品又は健康食品によると疑われる健康被害については、最寄りの保健所に連絡することとなっている。』
先の注記とはうって変わって、重要な注記です。
医薬部外品又は化粧品による健康被害ですが、法的な義務はないにせよ、自発的な協力が求められています。まあ、そうしたほうがいいですよねー。
次に、無承認無許可医薬品や健康食品によると疑われる健康被害は、保健所です。
出題実績はそんなにないですが、出しやすいので、チェックしておきましょう。
ひとくちコメント
そこそこ出ます。
一番出るのは、「なお、医薬品との因果関係が必ずしも明確でない場合であっても報告の対象となり得る。」のところです。
迅速な報告を担保するためかと思われます。とりあえず知らせておくってな次第ですね。
次に、報告対象となる副作用ですが、「身体の変調・不調、日常生活に支障を来す程度の健康被害(死亡を含む。)」が対象です。
ですから、すぐ治ったような軽い副作用なら、報告しなくていい、ってな次第です。救済制度と同様ですね。
最後に、「医薬品の過量使用や誤用等によるものと思われる健康被害」は、安全対策上必要があるときに、報告対象となります。つまりは、過量使用や誤用とかは、確定的な報告対象ではないわけですね。まあ、このあたり、難しく考えないでいいでしょう。
では、本文に戻ります。
「医薬品の副作用は、使用上の注意に記載されているものだけとは限らず、また、副作用の症状がその医薬品の適応症状と見分けがつきにくい場合(例えば、かぜ薬による間質性肺炎など)もある。」
「したがって、医薬品の販売等に従事する専門家においては、購入者等からの訴えに素直に耳を傾け、あるいはそのような副作用があるのでないかという、真摯な対応がなされることが重要である(※3)。」
注記‐(※3)
開ける
『総合機構ホームページでは、製薬企業から報告された、医薬品の副作用が疑われる症例に関する情報について公表しており、使用上の注意に記載されていなくても、それらの中に類似の事例があれば、医薬品による副作用である可能性が考慮されるべきである。なお、疑われる症例に関する情報は、因果関係が評価されているものでないこと、重複が含まれることに留意すべきである。』
そうですねーという注記です。
出題実績はないですが、一読だけはしておきましょう。
ひとくちコメント
一読しておけばいいでしょう。
では、本文に戻ります。
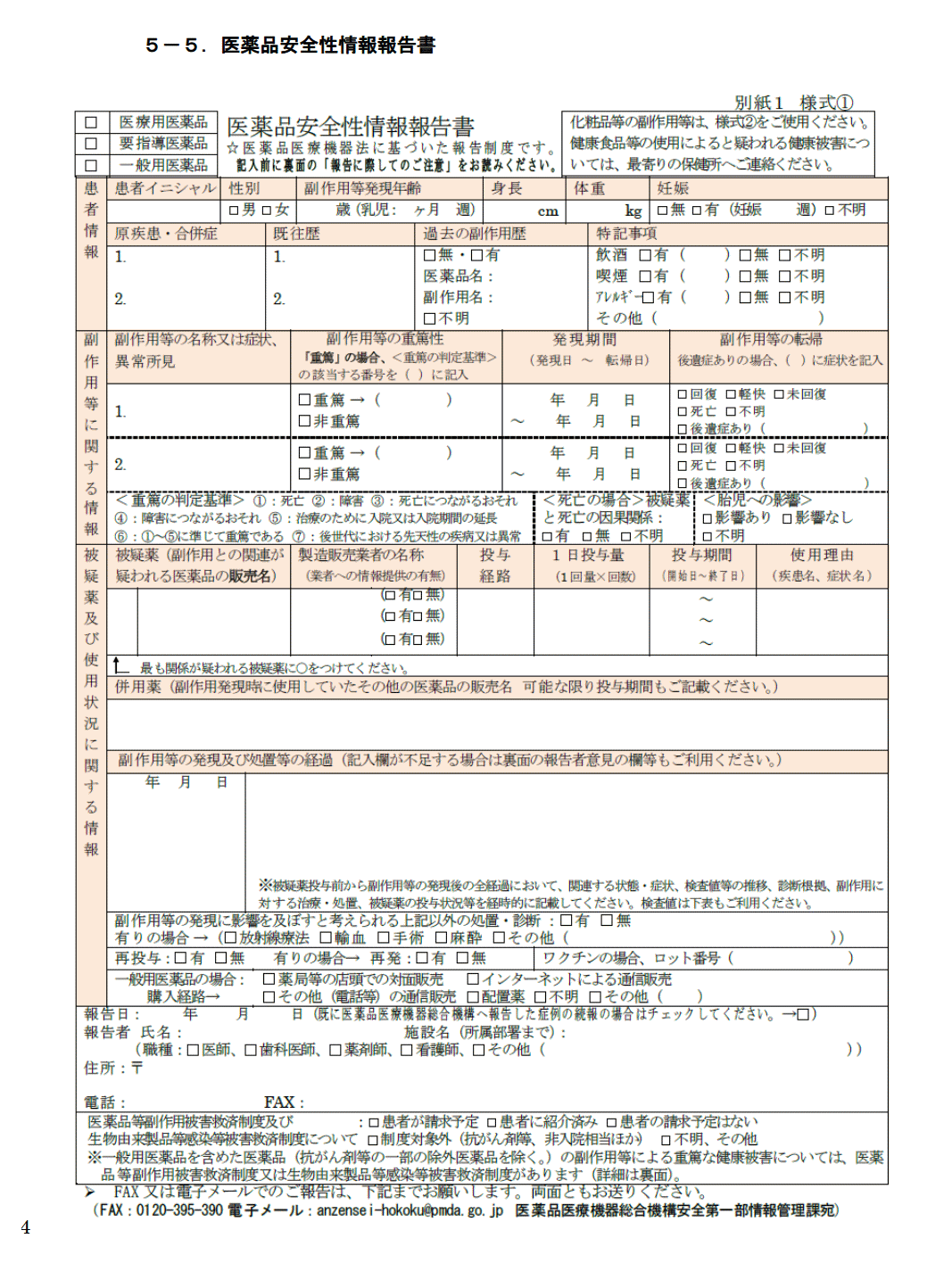
「報告様式(別表5-5)は、医薬品・医療機器等安全性情報と同様、総合機構ホームページから入手できる。」
「また、関係機関・関係団体の協力の下、医学・薬学関係の専門誌等にも掲載されている。」
ひとくちコメント
「報告様式」は、2~3回は見ておいてください。
氏名は、書かなくていいです。イニシャルですね。
性別欄はあります。身長体重年齢を書く欄あります。
ざっくりでいいので、押えておきましょう。結構、出ますよ。
では、本文に戻ります。
「報告様式の記入欄すべてに記入がなされる必要はなく、医薬品の販売等に従事する専門家においては、購入者等(健康被害を生じた本人に限らない)から把握可能な範囲で報告がなされればよい。」
「なお、複数の専門家が医薬品の販売等に携わっている場合であっても、当該薬局又は医薬品の販売業において販売等された医薬品の副作用等によると疑われる健康被害の情報に直接接した専門家1名から報告書が提出されれば十分である。」
「報告期限は特に定められていないが、保健衛生上の危害の発生又は拡大防止の観点から、報告の必要性を認めた場合においては、適宜速やかに、郵送、ファクシミリ又は電子メールにより、法の規定に基づき、報告書を総合機構に送付することとされている。」
「報告者に対しては、安全性情報受領確認書が交付される。」
「なお、本報告は、令和3年4月から、ウェブサイトに直接入力することによる電子的な報告が可能となった。」
ひとくちコメント
全部出ます。難しい内容じゃないので助かりますね。
試験問題は、オーソドックスで普通なものばかりです。
キチンと精読しておけば、十分です。
なお、繰り返しますが、下線部分・太文字部分は、ぜんぶ出題実績があるので、しっかり見ておいてください。読み飛ばしちゃダメですよ。
ページリンク
「Ⅱ 医薬品の安全対策」の医薬品による副作用等が疑われる場合の報告の仕方は、以上です。
「Ⅱ 医薬品の安全対策」も、これで終わります。
「Ⅲ 医薬品の副作用等による健康被害の救済」に続きます。
補足リンク
大元インデックス・・・「Webテキスト インデックス」
本章インデックス・・・「適正使用 インデックス」
本節インデックス・・・「医薬品の安全対策 インデックス」
こまごましたもの
登録販売者の独学方法については、「登録販売者の独学」を、参考にしてください。
登録販売者のブログ記事などは、「サイトマップ」に、挙げています。
★みんなとシェアする
第2節 安全対策
通読用
サイト内リンク
登録販売者
概要
独学シリーズ
対策シリーズ
勉強方法
過去問+解説
├チェック問題 過去問リスト
├漢方 過去問リスト
├生薬 過去問リスト
├全ブロック 試験問題 科目別
├「医薬品的な問題」過去問リスト
├「添付文書」過去問リスト
└「資料問題」過去問リスト